Lycée
Importance des exercices en sciences physiques pour les lycéens: Les exercices en sciences physiques sont essentiels pour préparer les élèves à leurs examens.
Ces activités contribuent à renforcer les connaissances théoriques et à développer des compétences pratiques et cognitives essentielles pour réussir..
Tronc Commun
Chimie
**Enoncé 1:
*Notion de mole.
Une cartouche de gaz contient V=700ml de butane C4H10 à l’état liquide.
Dans cet état sa masse volumique est ρ=0,6g/ml.
Lorsque l’on ouvre la cartouche le butane change d’état physique et on le récupère à l’état gazeux.
1/ Calculer la masse de butane liquide dans la cartouche.
2/ Quelle est la quantité de matière de butane dans la cartouche?
3/ Quel volume total de gaz peut-on espérer recueillir?
Données: M(C)=12g/mol; M(H)=1g/ml; M(O)=16g/ml
NA=6,02.1023 mol-1 ;Volume molaire V=24l/mol.
**Enoncé 2:
*Masse molaire et Mole .
Par définition,un vinaigre de 6° contient 6g d’acide acétique C2H4O2
dans 100g de vinaigre.
1/ Calculer la quantité d’acide acétique n contenu dans 100g de vinaigre à 6°.
2/ Calculer le volume V d’acide acétique contenu dans 100g de ce vinaigre.
Données: Masse volumique de l’acide acétique:
ρ=1,05g/L ; M(C)=12g/mol ; M(H)=1g/mol ; M(O)=16g/mol.
**Enoncé 3:
*La géométrie de la molécule chloroforme.
Le chloroforme est une substance anésthésiante dans les opérations chirurgicales.
La molécule du chloroforme est constituée,uniquement du carbone,du chlore et d’hydrogène.
Ses pourcentages atomiques en chlore et en carbone sont 60% et 20%.
On considère que la formule brute de cette molécule est de forme CxHyClz.
Avec x,y et z des nombres entiers.
1/ Trouver la relation entre x,y et z .Peut-on déduire ses valeurs?.
2/ La molécule de chloroforme ne contient qu’un seul atome de carbone .Déterminer les valeurs de x,y et z.
3/ Proposer une représentation de Lewis pour la molécule de chloroforme.
4/ Proposer une structure géométrique de la molécule.
**Enoncé 4:
*Composition d’ atome.
Déterminer la composition(nombre de protons,de neutrons et des électrons) des atomes suivants:
Nombre de masse: (58)Ni (9)Be (20)Ne (208)Pb (22)Ne (60)Ni (31)P (75)As (62)Ni
Données: Z(Be)=4 Z(Ne)=10 Z(P)=15 Z(Ni)=28 Z(As)=33 Z(Pb)=82
**Enoncé 5:
*Représentation symbolique d’un atome.
On considère le noyau de l’atome : ZAX
Avec A=2.Z +3
1/Sachant que le nombre de neutrons dans le noyau est N=20 Trouver la valeur des nombres Z et A.
2/ En se basant sur le tableau périodique donner le nom de l’élément chimique et sa représentation symbolique.
3/ Ecrire la structure électronique de cet atome.
4/ Définir la couche externe. Est-ce que cette couche est saturée ou non? Combien y a-t-il d’électrons de valence ?
Mécanique
**Enoncé 1:
*Comment on calcule la longueur initiale d’un ressort?
Quand on suspend une masse de 0,2kg à l’extrémité d’un ressort de raideur K=100N/m.
Sa longueur finale est 12cm ,quand on suspend une masse de 0,7kg, sa longueur finale est 17cm.
1- Donner le bilan des forces exercées sur la masse.
2- Déterminer la longueur initiale du ressort.
**Enoncé 2:
*Force de la terre sur un satellite.
Quelle est la force d’attraction exercée par la terre sur un satellite artificiel de masse m=600kg, qui tourne autour de la terre
à une altitude h=36000km de sa surface?
Données:
*Masse de la terre: M=6.1024kg.
*Rayon de la terre: R=6400km
*Constante d’attraction universelle : G=6,67.10-11(SI).
**Enoncé 3:
*Théorème de moments des forces.
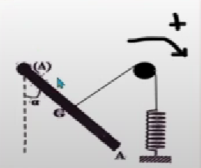
Une barre (OA) homogène de masse m=1kg et de longueur L pouvant tourner sans frottement autour d’un axe horizontal
passant par son extrémité O, est en équilibre comme l’indique la figure ci-dessous.
Le fil est fixé au centre G de la barre, passe sur la gorge d’une poulie et est fixé par l’autre extrémité à un ressort
verticale de raideur K ,à l’équilibre,le fil est normal à la barre, est α=30°.
1/ Faire l’inventaire des forces appliquées sur la barre(OA) et les representer sans souci d’échelle.
2/ Ecrire l’énoncé du théorème des moments.
3/ Par application de ce théorème, trouver l’intensité de la tension du fil.
4/ Déduire la valeur de la raideur du ressort sachant que son allongement est ∆l=5cm. g=10N/kg.
1ère BAC
Chimie
**Enoncé 1:
*Réaction d’hydrolyse(éthanoate de methyl)
On mélange dans un ballon 1,0 mol d’éthanoate de méthyle pur avec 1,0 mol d’eau distillée,
on ajoute quelques gouttes d’acide sulfurique concentré
et on chauffe à reflux le mélange réactionnel pendant un certain temps.
Une réaction chimique se produit.
A l’équilibre ,il reste 0,67 mol d’éthanoate de méthyle.
1/ Quel est le rôle de l’acide sulfurique ajouté?
2/ Citer deux caractéristiques de cette réaction.
3/ Ecrire l’équation de la réaction chimique étudiée en utilisant les formules semi-développées.
4/ Calculer la constante d’équilibre K associée à l’équilibre de cette réaction chimique.
**Enoncé 2:
*Calcul le nombre de molécules d’eau dans un Iceberg. Quantité de matière.
Un iceberg a un volume total V = 5000 m3 .
La masse volumique de la glace vaut 900kg/m3.
1/ Calculer la quantité de matière d’eau dans cet iceberg.
2/ En déduire le nombre de molécules d’eau dans cet iceberg.
On donne: M(H) =1 g/mol M(O)=16g/mol. NA= 6,02 .1023 mol-1.
**Enoncé 3:
*Demi-equation redox..
Ecriture des demi-équations:
Exemple des couples:
1/ NO3/NO
2/ CH3COOH/C2H5OH
Mécanique
**Enoncé 1:
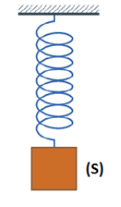
*Equilibre d’un corps solide.
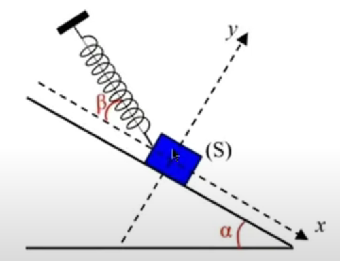
Un solide(S) de masse m=0,2 kg est maintenu en équilibre sur un plan incliné parfaitement lisse d’inclinaison α=30° par rapport à l’horizontale par l’intermédiaire d’un ressort de constante de raideur K=40N/m.
L’axe du ressort fait un angle ß=20° avec le plan incliné.
1/ Faire l’inventaire des forces appliquées au solide (S) et les représenter sur le schéma.
2/ Exprimer l’allongement ∆L du ressort ,en fonction de m,g,α,Ketß.
3/ Exprimer R l’intensité de la réaction du plan en fonction de m,g,α,K, ∆L et ß.
4/ Calculer la valeur de ∆L puis la valeur de R.
Donnée : g= 10N/kg.
**Enoncé 2:
*Détermination de la quantité d’électricité et la durée de passage de courant.
A/ Un électrolyseur est traversé par une quantité d’électricité de charge 72000 C pendant 2h.
Quelle est l’intensité du courant dans les conducteurs du circuit?
B/ On recharge durant 12 h une batterie d’accumulateurs avec un courant constant d’intensité 5A.
Quelle quantité d’électricité correspond à cette charge?
C/ Sur une batterie de téléphone portable,il est indiqué 1,3Ah.
Le télephone consomme en moyenne 0,08A. Calculer la durée au bout de laquelle la batterie est complètement déchargée?
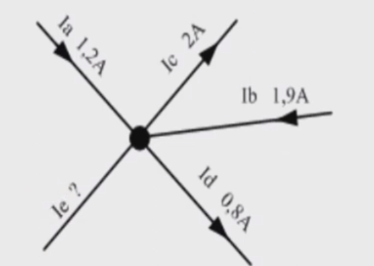
D/ Dans un noeud de 5 conducteurs on mesure la valeur de l’intensité de 4 conducteurs suivant le dessin suivant:
Calculer la valeur Ie du cinquième conducteur et son sens?
2ème BAC
Chimie
**Enoncé 1:
*Acide et base selon Bronsted.
On considère les espèces chimiques suivantes:
C6H5CO2H , HCOO– ,HO– , NH4+ ,HF , HCOOH , F– ,NH3 , C6H5CO2–, H2O:
1/ Former les couples acide/base.
2/ Ecrire les équations des réactions acido-basiques avec l’eau des ces espèces chimiques.
**Enoncé 2:
* Les demi-équations du couple oxydoréduction.
Ecrire les demi-équations des couples suivants :
1/ Cr2O72- / Cr3+.
2/ MnO4– / Mn2+.
**Enoncé 3:
* Comment on différencier entre la Réaction lente et la Réaction rapide ?
On considère l’oxydation lente de l’acide oxalique par les ions permanganate.
A l’instant t=0 on mélange un volume de Vo= 25mL de la solution permanganate de potassium,
de concentration Co=0,01mol/L et un volume de Vr=20mL de l’acide oxalique de concentration Cr=0,1 mol/L.
On ajoute un volume de 5 mL d’acide sulfurique pour acidifier la solution.
L’ion permanganate(MnO4–) et l’acide oxalique (H2C2O4),appartiennent aux couples redox suivants:
MnO4–/Mn2+ CO2/H2C2O4
1/ Ecrire les demi-équations électroniques relatives aux couples et établir l’équation de la réaction.
2/ Déterminer les quantités de matière des réactifs mis en présence.
3/ Dresser le tableau descriptif,déduire deux réactifs mis en présence, quel est celui qui constitue le facteur limitant?
4/ Quelle est la concentration des ions manganèse en fin de réaction?
5/ L’ion (MnO4–)en solution est de couleur violette.
L’acide oxalique et l’ion manganèse en solution sont incolores,comment peut-on mettre en évidence l’évolution de la réaction.
**Enoncé 4 :
* Calcul du pH de deux bases Calcul du pH de deux bases fortes..
On mélange V1=100mL d’une solution d’hydroxyde de sodium (NaOH)de concentration C1=0,1mol/L avec V2=50mL d’une solution d’hydroxyde de potassium (KOH) de concentration C2=0,2mol/L.
*Calculer le pH du mélange obtenu.
Ondes
**Enoncé :
*Propagation lumineuse– Danger du rayon laser..
Un pointeur laser utilisé par un conférencier,émet un faisceau lumineux de fréquence V=422THz et de puissance P=2mW
par une ouverture circulaire de diamètre d1=2mm,ilproduit une tache lumineuse de diamètre d2=10mm sur un écran situé à une distance D=10m de l’ouverture.
Donnée: C=3.108m/s.
1/ Calculer la longueur d’onde de la lumière émise par le laser dans l’air.
Quelle est la couleur du faisceau?
2/ Calculer la valeur de l’angle Ɵ appelé divergence du faisceau.
3/
a- Quelle est l’aire A de la tache lumineuse obtenue sur l’écran?
b- On admet que toute la puissance émise est transportée jusqu’à l’écran.
Calculer la puissance lumineuse par unité de surface reçue par l’écran.
c- Le faisceau est dangereux pour l’oeil humain si la puissance reçue par unité de surface est supérieure = 20W/m2..Conclure.

Mécanique
**Enoncé 1:
*Application de la 2ème loi de Newton (Mécanique).
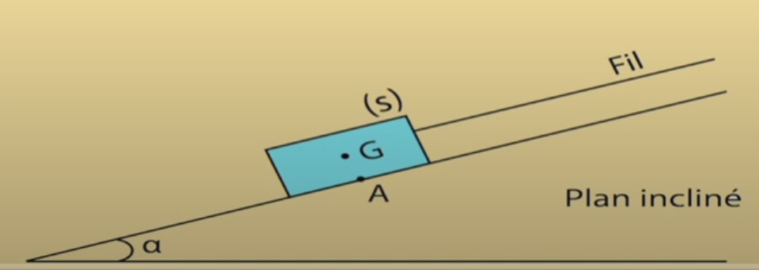
Un solide (S) de masse m= 1kg est posé sur un plan incliné d’angle α=30° par rapport à l’horizontale.
On applique sur(S) à l’aide d’un fil inextensible et de masse négligeable, une force T constante de direction parallèle à la ligne de plus grande pente du plan incliné.
Le solide glisse alors sur le plan incliné sans vitesse initiale.
La valeur de l’accélération de centre d’inertie G de (S) est : a0=1m/s2.
Les deux composantes RT et RN de la force R exercée par le plan incliné sur (S) sont la relation suivante : RT= RN/4 g= 10 m/s2
1-Calculer l’intensité de RN , en déduire l’intensité de R .
2- Déterminer l’expression de l’intensité de la tension T du fil en fonction de m , g , a0 , α et RT. Calculer sa valeur.
3- Calculer l’angle de frottement φ.
4- Ecrire l’équation horaire du mouvement de G,en prenant comme origine des dates le point o, origine du repère d’espace R(o,i,j ).
**Enoncé 2:
*Chute d’un corps dans un fluide.
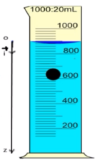
Afin de déterminer quelques caractéristiques du mouvement de chute d’une bille dans un liquide visqueux,
On réalise l’expérience suivante :
On remplie une éprouvette graduée par un liquide visqueux et transparent, puis on libère une bille sans vitesse initiale de masse 20g, est soumise à une force de frottement f = k VG.
En appliquant la 2ème loi de Newton, montrer que l’équation différentielle vérifiée par la vitesse s’écrit sous la forme :
dVG/dt+1/(σ ) VG=A
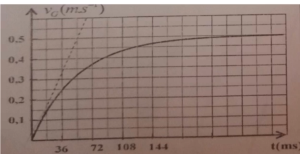
Déterminer graphiquement la valeur de la vitesse limite Vlim et la valeur de σ.
Trouver la valeur de k.
L’équation différentielle s’écrit :
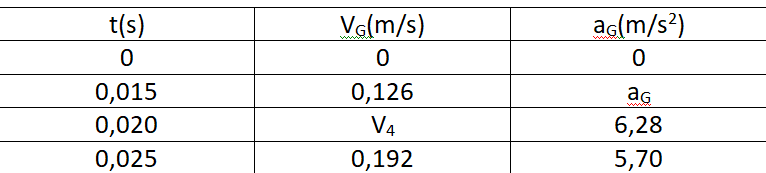
dVG/dt = 9,26 – 18,52 VG
En utilisant la méthode d’Euler et les données du tableau déterminer a3 et V4.